CDE生物制品审评分析报告
根据药智数据最新统计,2022年10月份CDE共承办新的药品注册申请以受理号计有973个(复审除外,下同)其中化药受理723个,中药受理97个,生物制品受理153个;2022年5-10月各类药品注册申请受理情况详见图1。
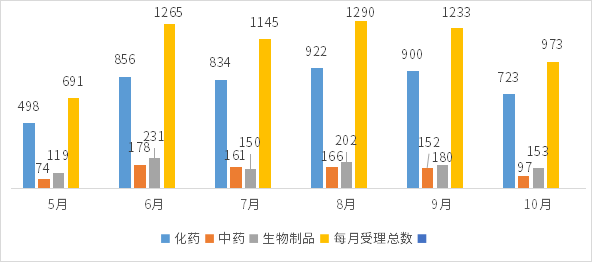
图1 2022年5-10月CDE药品受理情况
2022年10月份(注:状态开始时间(药智)从2022年10月1日至2022年10月31日)完成审评的受理号共892个,其中化药受理652个,中药受理118个,生物制品受理122个;2022年5-10月各类药品完成审评情况详见图2。
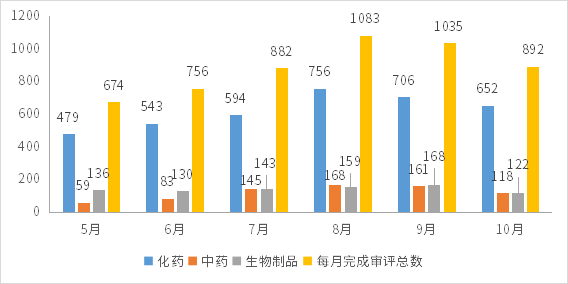
图2 2022年5-10月CDE药品完成审评情况
生物制品审评情况
1 生物制品受理情况
10月份CDE承办新的生物制品注册申请受理号共计153个,新药51个,补充申请62个,进口35个(其中包括一次性进口21个),进口再注册5个;2022年5-10月CDE生物制品各申请类型受理情况详见图9。
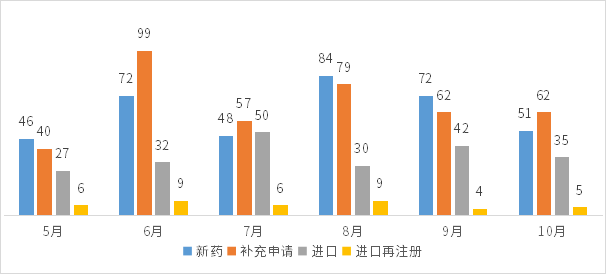
图9 2022年5-10月CDE生物制品各申请类型受理情况
01.生物制品1类新药申报情况
10月共39个生物制品1类新药受理号获得承办,其中上市申请1个,临床试验申请38个,目前都已经进入相应序列排队待审;下表为10月新承办的生物制品1类创新药。
表7 2022年10月新承办的生物制品1类新药
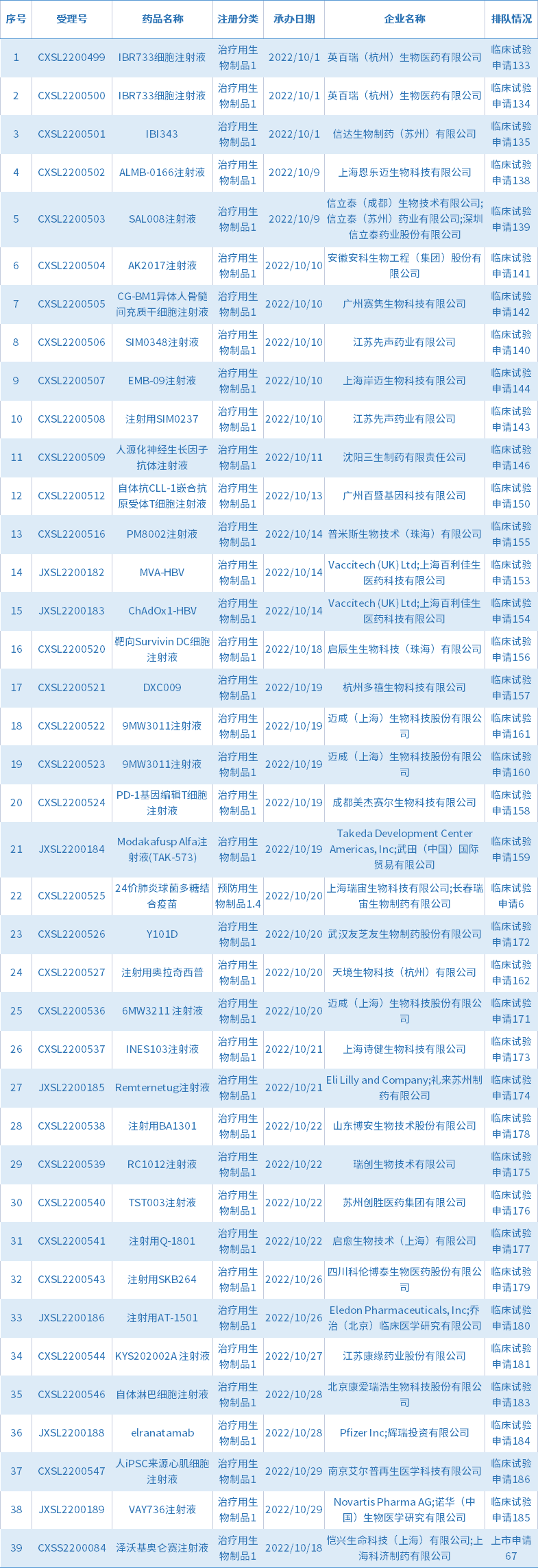
注:排队序号截止至2022年11月02日。
2 生物制品完成审评情况
10月份CDE完成审评的生物制品注册申请122个(以受理号计),其中新药申请受理号46个,进口受理号19个,补充申请53个;以审评任务类别统计(以受理号计),临床试验申请48个,上市申请12个,补充申请53个;2022年10月CDE生物制品各审评任务类别完成审评情况详见图10;
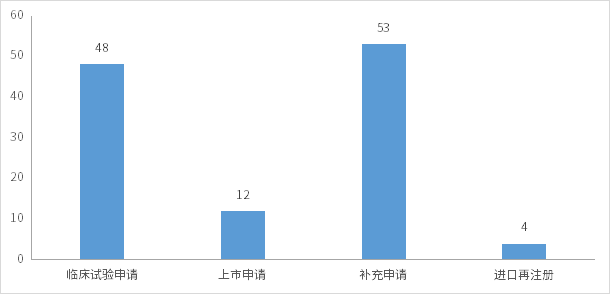
图10 2022年10月CDE生物制品各审评任务类别完成审评情况
1.生物制品新药获批上市情况
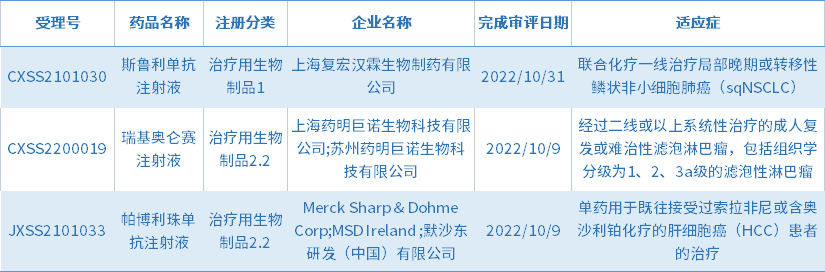
10月共3个生物制品获批上市,都是新增适应症;下表为10月获批上市生物制品新药信息。
表8 2022年10月获批上市生物制品信息

用户登录
还没有账号?
立即注册