-
2021-07-19
2021-07-19 近日,辉瑞(Pfizer)和BioNTech联合宣布,美国FDA已经授予其为mRNA新冠疫苗递交的生物制品许可申请(BLA)优先审评资格,用于在16岁以上人群中预防COVID-19。这一申请的PDUFA日期为2022年1月。 辉瑞和BioNTech在今年5月完成这一BLA的滚动申请。它是基于新冠疫苗在关键性3期临床试验中的数据,试验数据显示接种第二剂后6个月内,疫苗表现出良好的防护效力和安全性。它已经获得美国FDA授予的紧急使用授权(EUA),但是尚未获得FDA的完全批准。 在今年5月10日,美国FDA扩展了这一疫苗EUA,授权它用于在12-15岁青少年中预防查看更多 -
2021-07-19
2021-07-19 7月17日,康希诺发布2021年半年度业绩预告,预计上半年实现营业收入20-22亿元,同比增加49532.59%至54495.85%;预计上半年实现归母净利润9-10.5亿元,同比扭亏为盈。这也是康希诺自2009年成立以来,首次真正意义上实现盈利。 根据公告,本次盈利的主要原因在于其重组新型冠状病毒疫苗(5型腺病毒载体)(Ad5-nCoV,商品名:克威莎)的大卖。 2021年2月,国家药监局附条件批准康希诺的腺病毒载体新冠疫苗上市注册申请,这是我国首个获批的腺病毒载体新冠疫苗,同时该疫苗还获得了墨西哥、巴基斯坦等国的紧急使用授权。公告表示,这对康希查看更多 -
2021-07-19
2021-07-19 导读:即将进入III期临床! 全球战“疫”已历时一年半,已有14款新冠疫苗获批紧急使用或上市。然新冠病毒仍旧在全球加剧蔓延,这场人类历史上百年难遇的传染性疾病,仍未到达人类最终胜利的拐点。作为预防和控制传染病最有效、最经济的手段,新冠疫苗的研发进展一直倍受关注。 又一款国产新冠疫苗取得进展 丽珠生物重组蛋白疫苗II期试验数据亮眼 据药智网获悉,近日,《中华医学杂志》发布了上市公司丽珠集团旗下丽珠生物全资子公司丽珠单抗的新冠疫苗V-01的II期临床试验数据,结果进一步证实V-01的免疫原查看更多 -
2021-07-19
2021-07-19 导读:用于在18岁以上成人中预防由肺炎链球菌血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F和33F引起的侵袭性疾病。 当地时间7月16日,默沙东宣布美国FDA批准其肺炎球菌15价结合疫苗Vaxneuvance上市,用于在18岁以上成人中预防由肺炎链球菌血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F和33F引起的侵袭性疾病。Vaxneuvance曾获得美国FDA授予的优先审评资格。 这一批准是基于7项在成人中评估Vaxneuvan查看更多 -
2021-07-19
2021-07-19 导读:双方以“mRNA 狂犬病疫苗项目”作为第一个正式合作项目展开友好合作。 7月19日,康泰生物发布公告,公司全资子公司北京民海生物科技有限公司于近日与嘉晨西海(杭州)生物技术有限公司签署了《战略合作协议》,双方就使用mRNA平台技术在人用传染病疫苗项目领域开展合作,共同研发、申报、生产mRNA平台技术在人用传染病疫苗方向的产品。 此前,双方已完成mRNA人用狂犬病疫苗部分项目的有效性验证,验证结果表明嘉晨西海的mRNA平台技术具备人用传染病疫苗开发的基础。 康泰生物表示查看更多 -
2021-07-15
2021-07-15 按照协议,国药集团中国生物将从7月开始向COVAX参与国提供疫苗。 预计首个合同将供应1.7亿剂北京生物制品研究所新冠灭活疫苗,通过“新冠肺炎疫苗实施计划”(COVAX)分配给全球参与国。 北京,2021年7月7日,国药集团中国生物北京生物制品研究所与全球疫苗免疫联盟(Gavi)签署了首个新冠灭活疫苗预购协议(APA)。该协议将为“新冠肺炎疫苗实施计划”(COVAX)参与国家提供多达1.7亿剂疫苗。 按照协议,北京生物制品研究所将从2021年第三季度开始首次供应6000万剂疫苗。Ga查看更多 -
2021-07-15
2021-07-15 北京时间7月12日,国药集团中国生物、G42集团与塞尔维亚新冠疫苗合作签约仪式在中国北京、阿联酋阿布扎比、塞尔维亚贝尔格莱德三地以视频方式举行。塞尔维亚总理阿娜·布尔纳比奇、国药集团中国生物董事长杨晓明、阿联酋G42集团CEO肖鹏代表三方共同签署新冠灭活疫苗合作备忘录,启动塞尔维亚新冠疫苗原液分装项目建设。塞尔维亚产新冠疫苗将会在本国疫情防控及全球共同战疫中发挥重要作用。 阿娜·布尔纳比奇总理在致辞中表示,感谢习近平主席、中国政府和人民为塞抗疫斗争提供的宝贵支持和帮助。没有中国的经验、医疗物资和设备,没有国药集团按时足量向塞供应查看更多 -
2021-07-15
2021-07-15 导读:复星医药mRNA新冠疫苗来自与BioNtech合作获得大中华区权益。 据财新网报道,2021年7月14日,在香港上市的复星医药董事长兼CEO吴以芳在股东大会上回复投资人问询时表示,中国国家药监局对mRNA新冠疫苗“复必泰”的审定工作已经基本完成,专家评审已经通过了,目前正在加紧进行行政审批阶段。 “我们和药监局等部门的沟通很顺畅,有关部门对疫苗审批也是一分一秒抓得很紧。”复星医药董事长兼CEO吴以芳说,在供货问题上,复星医药已经与BioNTech提前启动生产准备工作,复必泰疫苗一旦查看更多 -
2021-07-14
2021-07-14 2021年7月13日,Affinivax和安斯泰来(Astellas Pharma)公司公布,其联合开发的创新肺炎球菌疫苗ASP3772在2期临床试验中获得积极结果。ASP3772采用Affinivax专有的多抗原呈现系统(MAPS)技术平台,可以同时呈现多糖与蛋白抗原,从而对多种肺炎球菌血清型提供更广泛与强效的免疫保护(B细胞+T细胞)。2期试验结果表明,ASP3772具有良好的耐受性。此外,ASP3772激发针对24种肺炎球菌多糖抗原的抗体反应,对疫苗呈现的2种保守肺炎球菌蛋白抗原也产生了抗体反应。 基于本次2期试验的积极结果,美国FDA已经授予ASP3772查看更多 -
2021-07-14
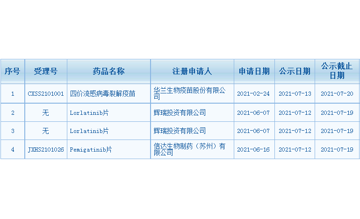
2021-07-14 导读:包括信达生物FGFR抑制剂、辉瑞第三代ALK抑制剂、华兰生物四价流感病毒裂解疫苗(儿童剂型)。 根据中国国家药品监督管理局(NMPA)药品审评中心(CDE)最新公示显示,辉瑞第三代ALK抑制剂Lorlatinib片、信达生物FGFR抑制剂pemigatinib片和华兰生物四价流感病毒裂解疫苗拟纳入优先审评。 来源:CDE官网 Lorlatinib片 信达生物FGFR 1/2/3抑制剂pemigatinib片,以“符合附条件批准的药品”拟纳入优先审评,拟定适应症查看更多






用户登录
还没有账号?
立即注册